概述
全面的蛋白质序列和结构分析软件,可与Nova蛋白质结构预测和建模工具集成。
找到一个集成了成功蛋白质分析所需所有组件的软件包可能是一项挑战。了解蛋白质的结构对于理解蛋白质的功能至关重要,但许多蛋白质分析工具忽略了蛋白质结构分析与蛋白质序列的生物物理特性之间的重要联系。
LasergeneProtein 超越其他蛋白质分析工具,提供灵活、丰富的蛋白质结构3D图形表示,与序列和结构分析完全集成,蛋白质设计工具可让您轻松预测蛋白质稳定性,并通过集成预测蛋白质结构具有无与伦比的准确性使用我们的 Nova应用程序。
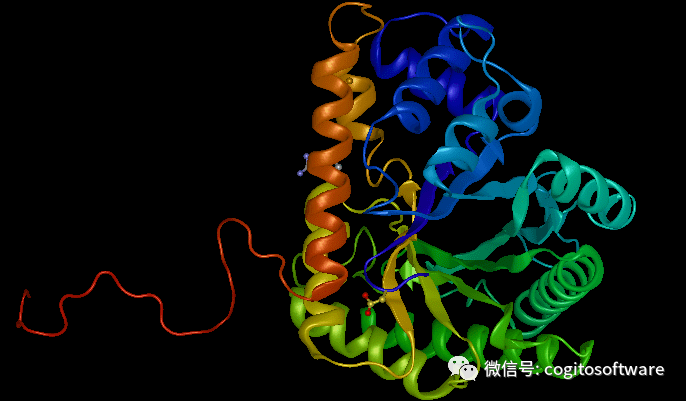
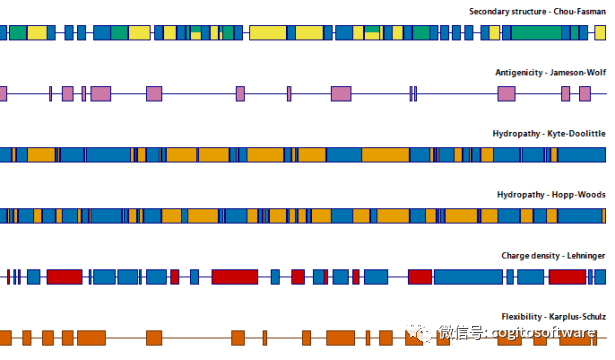
LasergeneProtein 工作流程
抗体建模*
使用NovaFoldAntibody 在几分钟内根据序列数据预测高度准确的抗体模型。
抗体建模是抗体设计和优化的重要工具,准确性至关重要。许多抗体建模工具仅依赖于同源建模,但 NovaFoldAntibody的独特算法通过结合框架区的同源建模和基于片段或高变环区域的从头建模来生成抗体和抗体片段的模型,从而实现高度准确的抗体结构预测。只需提供轻链、重链或两者的序列,NovaFoldAntibody 将返回一份带注释的报告,其中包括预测的抗体模型、最高可能性的重链和轻链模板以及CDR环位置的注释。通过 Protean3D(LasergeneProtein 的一部分)中的注释轻松查看抗体建模结果,它允许您完全自定义渲染以帮助可视化,或准备要导出的出版质量图像。使用 NovaFoldAntibody 进行的抗体建模也可以与NovaDock结合使用,以预测抗体-抗原复合物的结构和结合。
表位预测
使用Protean3D 仅使用基于序列的信息即可准确执行B细胞表位预测。
B细胞表位(抗体识别的抗原的一部分)本质上是构象的;然而,对于没有已知 3D结构的蛋白质来说,准确的表位预测是困难的。Protean3D 是LasergeneProtein 的一部分,它采用机器学习方法,提高了仅使用基于序列的信息执行B细胞表位预测的能力,与其他领先的表位预测方法相比,提供了更好的整体预测准确性。Protean3D 使您能够查看序列和结构上的预测表位和抗原区域,并将预测与其他特征(例如表面概率)进行比较。轻松在结构周围创建分子和溶剂可及的表面,查看相对于蛋白质表面的预测表位,查看预测抗原区域的置信度分数,并更改序列和结构上预测表位的外观,以优化可视化和出版质量的图像。
蛋白质对接*
NovaDock探索对接时蛋白质的灵活性,从而实现更准确的蛋白质-蛋白质相互作用预测。
对蛋白质-蛋白质对接相互作用进行建模通常比预测单个蛋白质的结构更困难,并且由于其复杂性,准确性可能是一个问题。NovaDock能够利用SwarmDock(CAPRI盲对接实验中验证的顶级算法之一)预测任意两个结合伙伴的蛋白质-蛋白质对接相互作用。NovaDock利用SwarmDock算法探索对接时蛋白质的灵活性,从而实现更准确的预测。只需提供您的配体和受体 PDB或结构文件,并在需要时提出结合配偶体之间的特定残基接触。然后,NovaDock将预测多蛋白复合物的三维结构,并为每个模型提供能量评分、簇大小和配体接触数量以供分析。
蛋白质序列分析
在一款易于使用的应用程序中使用Protean3D 进行全面的蛋白质序列分析!
蛋白质序列分析对于研究和预测蛋白质功能和结构至关重要,但蛋白质序列分析工具通常缺乏解释所需的可视化组件,或者需要额外的工具进行下游分析。Protean3D 中提供的蛋白质序列分析工具提供了所应用方法的优雅图形表示,使分析生物物理特性、预测B细胞表位等二级结构、计算表面概率、执行氨基酸组成分析等变得简单。更重要的是,Protean3D是一个完整的蛋白质序列分析软件包,这意味着在分析和注释蛋白质序列后,您可以立即进行蛋白质结构分析,以及预测蛋白质结构、进行抗体建模或评估蛋白质-蛋白质对接互动。使用 Protean3D 在一款易于使用的应用程序中提供全面蛋白质序列分析所需的一切!
蛋白质稳定性预测
使用LasergeneProtein 的蛋白质设计软件在几分钟内即可执行基本的蛋白质稳定性预测。
蛋白质稳定性预测对于优化蛋白质功能研究至关重要,但许多提高溶解度和表达的标准方法通常由于降解或热力学不稳定而无效。我们的蛋白质设计软件是 LasergeneProtein 的一部分,包括蛋白质突变稳定性预测工具,该工具使用确定性蛋白质设计算法来查找全局最小能量构象(GMEC)。这使您可以在蛋白质结构的残基水平上进行改变,并预测与原始结构相比这些改变是否可能稳定或不稳定,这是PCR定点诱变的有益过程。我们的蛋白质稳定性预测工具还可以通过执行计算丙氨酸扫描或丝氨酸扫描来检测热点、其变体破坏结构稳定性的残基,从而轻松搜索对蛋白质稳定性重要的氨基酸位置。使用 LasergeneProtein 的先进蛋白质设计软件可在几分钟内进行准确的蛋白质稳定性预测!
蛋白质结构比对
使用Protean3D 轻松执行整个大分子结构或选定区域的蛋白质结构比对。
同源蛋白质通常具有相似的结构。蛋白质结构比对软件可以成为通过比较结构之间的形状和3D构象来识别这些相似性的有价值的工具。蛋白质结构比对也是将 NovaFold预测模型与蛋白质数据库中的模板结构进行比较的宝贵工具。Protean3D 是LasergeneProtein 的一部分,可以轻松识别两个或多个结构之间的相似区域,而与序列相似性无关。只需添加结构文件或打开 NovaFold结果,然后从TM-Align或jFATCAT刚体对齐算法中进行选择。在进行蛋白质结构比对后,评估比对结构的 RMSD值,以确定它们之间的差异。然后,在 Protean3D 中自定义可视化的渲染,以准备要发布的蛋白质结构比对图像。
蛋白质结构分析
在一款用户友好的应用程序中使用Protean3D 进行完整的蛋白质结构分析!
了解蛋白质的结构对于理解蛋白质的功能至关重要,但当今可用的许多蛋白质结构分析工具缺乏有效分析所需的高质量可视化组件,并且错过了蛋白质结构分析与蛋白质序列的生物物理特性之间的关键联系。Protean3D 是LasergeneProtein的一部分,它通过创建美观、灵活、丰富的蛋白质图形表示并在单个应用程序中提供与蛋白质序列分析和结构预测工具的完全集成来消除这些挑战。我们的蛋白质结构分析工具可以轻松分析您感兴趣的蛋白质结构或引入突变并查看对蛋白质结构的影响。三维蛋白质结构可视化的无限可能性提供了一种生成出版质量图像的简单方法。使用 Protean3D 在一款用户友好的应用程序中提供全面蛋白质结构分析所需的一切!
蛋白质结构预测*
创建高度准确的蛋白质模型,这是通过标准建模方法无法实现的。
根据独特的氨基酸序列预测蛋白质3D结构非常重要,因为拥有蛋白质结构模型可以更好地理解蛋白质的工作原理,这可以让我们创建关于如何影响它、控制它或修改它的假设。许多蛋白质结构预测工具仅依赖于同源建模,这仅适用于与蛋白质数据库中的蛋白质序列具有高度序列相似性的蛋白质。
相比之下,NovaFold和NovaFoldAI 使用两种不同的获奖算法来创建高精度、完整的蛋白质3D原子模型,这是通过标准建模方法无法实现的。
-
NovaFold利用屡获殊荣的I-TASSER蛋白质结构预测算法,该算法结合了线程和从头开始折叠技术。NovaFold比单独的序列相似性发现更远的关系,从而提高了预测结构的质量和准确性。
-
NovaFoldAI 使用DeepMind(最近CASP14挑战赛的获胜者)的AlphaFold2 算法来预测距离并使用深度多序列比对作为输入来创建二面体图。该算法不直接使用模板来放置原子坐标,但可以使用模板作为地图构建过程的一部分。
LasergeneProtein 应用程序
Protean3D
蛋白质序列和结构分析
Protean3D 提供灵活、丰富的蛋白质结构3D图形表示,结合了序列和结构分析以及蛋白质稳定性预测工具。
NovaFold*
蛋白质结构预测
NovaFold是蛋白质结构预测软件,可与LasergeneProtein 配合使用,为具有先前未知结构的蛋白质构建准确、完整的3D原子模型。
NovaFoldAntibody*
抗体建模
NovaFoldAntibody 软件利用同源建模和从头开始循环预测的组合生成高度准确的抗体和抗体片段模型。
NovaDock*
蛋白质-蛋白质对接
NovaDock是一款高分辨率蛋白质-蛋白质对接应用程序,可预测任意两种蛋白质之间的原子相互作用。
对比DNASTARLasergene 软件包
|
LasergeneMolecular Biology |
LasergeneGenomics |
LasergeneProtein |
DNASTARLasergene (最受欢迎) |
|
|
包含的应用程序 |
||||
|
SeqBuilderPro |
|
|
||
|
SeqManUltra |
|
|
|
|
|
MegAlignPro |
|
|
||
|
GeneQuest |
|
|
||
|
GenVision |
|
|
||
|
SeqNinja |
|
|
||
|
SeqManNGen |
|
|
||
|
ArrayStar |
|
|
||
|
GenVisionPro |
|
|
||
|
Protean3D (每个Nova应用程序+1预测) |
|
|
||
|
DNASTARNavigator |
|
|
|
|
-
模型
+关注
关注
1文章
3226浏览量
48806 -
应用程序
+关注
关注
37文章
3265浏览量
57677 -
蛋白质
+关注
关注
0文章
25浏览量
7981
原文标题:DNASTAR Lasergene Protein
文章出处:【微信号:哲想软件,微信公众号:哲想软件】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐




 LasergeneProtein工作流程
LasergeneProtein工作流程










评论