电解液是锂离子电池四大主材之一,有锂离子电池的“血液”之称,电解液主要由有机溶剂、电解质锂盐及不同类型的添加剂组成。
其中有机溶剂是电解液的主体部分,锂离子电池常用溶剂有碳酸乙烯酯(EC)、碳酸二乙酯(DEC)、碳酸二甲酯(DMC)、碳酸甲乙酯(EMC)等,其中EC与一种链状碳酸酯的混合溶剂是锂离子电池优良的电解液,如EC+DMC、EC+DEC等。
LiPF6是最常用的电解质锂盐,其电导率高,内阻小,充放电速度快,但对水分和HF极其敏感,极易发生反应,且不耐高温,80℃~100℃会发生分解,生成五氟化磷和氟化锂,而合适的添加剂可有效降低电解液中的微量水和HF,进而有效抑制LiPF6水解反应的发生,目前关于添加剂的种类研究颇多,不同厂家对电池的性能及要求有差异,所选择的添加剂类型也会有所差异,通常添加剂的作用除了降低电解液中水分和HF的作用外,还有改善界面稳定性、高低温性能及防过充、过放等方面的应用。
如图1为几种常见溶剂、添加剂和脱溶离子还原电位的计算结果【1】。
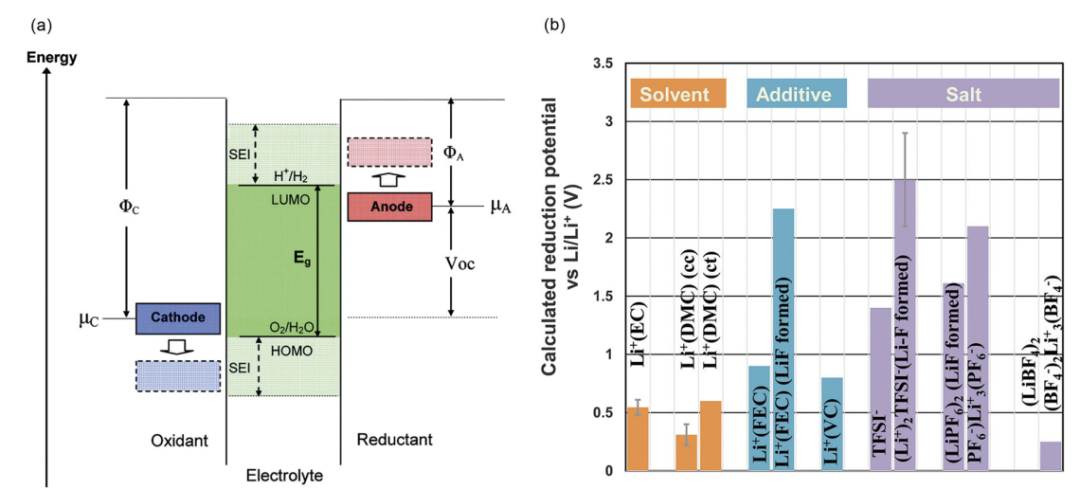
图1 a.电解液开路能量图示意图;
b. 几种常见溶剂、添加剂和脱溶离子还原电位的计算结果¹
传统碳酸酯溶剂的电化学窗口较窄、一般低于4.3V。电压升高后,溶剂会发生分解,而且溶剂还会与高电压状态的正极发生副反应,致使三元材料中的过渡金属溶出,并产生大量气体,大幅降低电池的容量甚至安全性。对于NCM三元正极,Ni、Co、Mn的氧化态分别为+2、+3和+4价。
在充电时,锂离子从正极脱嵌,因此Ni将由+2价转变为+3价乃至+4价,同时正极会与电解质反应生成一层固体电解质界面(CEI层),CEI层对正极会起到保护作用,阻碍正极与电解液的进一步反应,提高正极在脱锂状态下的稳定性。但CEI膜的形成,也会同时造成电池阻抗增加、倍率衰减、容量衰减等问题。
因此,电解液体系对锂离子电池产气的影响至关重要,电池内部产气直接增加电池使用安全风险,故电池产气是考察电池质量和可靠性重要指标之一。现阶段国内外对于锂离子电池产气行为的研究主要集中在正极和电解液两个方面,而且添加剂的作用效率与正极材料的类型和组成密切相关。本文结合NCM正极对Li的半电池体系分析不同电解液体系对电池产气行为及产气成分的影响。
实验设备与测试方法
1.实验设备:型号GVM2200(IEST元能科技),测试温度范围20℃~85℃,支持双通道(2个电芯)同步测试,设备外观如图2所示。
2.测试参数:70℃温度条件下, 0.3C CC to 4.4V。
3.测试方法:选取不同的电解液体系(Electrolyte1& Electrolyte2,其中Electrolyte2在Electrolyte1的基础上加入部分添加剂)手套箱内组装成单层叠片电芯,对电芯进行初始称重m0,将待测电芯放入设备对应通道,开启MISG软件,设置各通道对应电芯编号和采样频率参数,软件自动读取体积变化量,测试温度,电流,电压,容量等数据。
气体成分测试采用GC-2014C气相色谱仪,对过充后的电芯在手套箱中取出1mL的气体,分别使用TCD和FID两种检测器对不同类型的气体浓度进行测试,可测气体类型如图3所示。
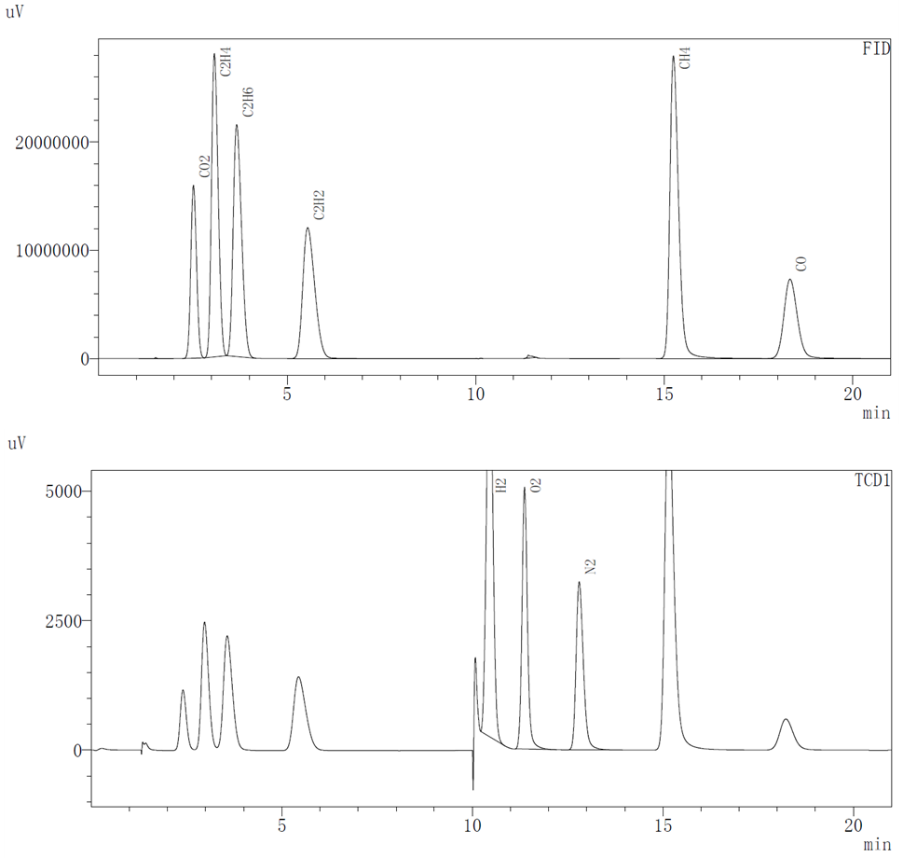
图3. FID和TCD检测器可测试的气体成分
不同电解液体系原位产气及成分分析
1.充电电压曲线和单位体积变化曲线分析
两种不同电解液体系电芯的电压与单位体积变化曲线如图4所示,从不同电解液Electrolyte1、Electrolyte2电芯曲线上可以看出,两种电解液体系的充电电压曲线和体积变化曲线均有明显差异。
从单位体积变化曲线上看,Electrolyte1体系电芯整个充电阶段始终保持着较高的体积变化速率,而Electrolyte2体系电芯在充电初期保持一个较低的体积变化速率,充电电压达到4.2V左右,电芯SOC达到约80%后,体积变化速率才明显增大,这说明Electrolyte2体系中添加剂的加入可有效降低NCM对Li电芯的单位产气速率;
从电压曲线上看,相比Electrolyte1体系,Electrolyte2体系电芯的充电平均电压更低,如果忽略电芯本身组装的差异, Electrolyte2体系中添加剂的加入,可能使电芯NCM正极与电解液添加剂发生反应生成界面膜,阻止电解液与正极材料的持续反应,电芯的平均电压也较低。
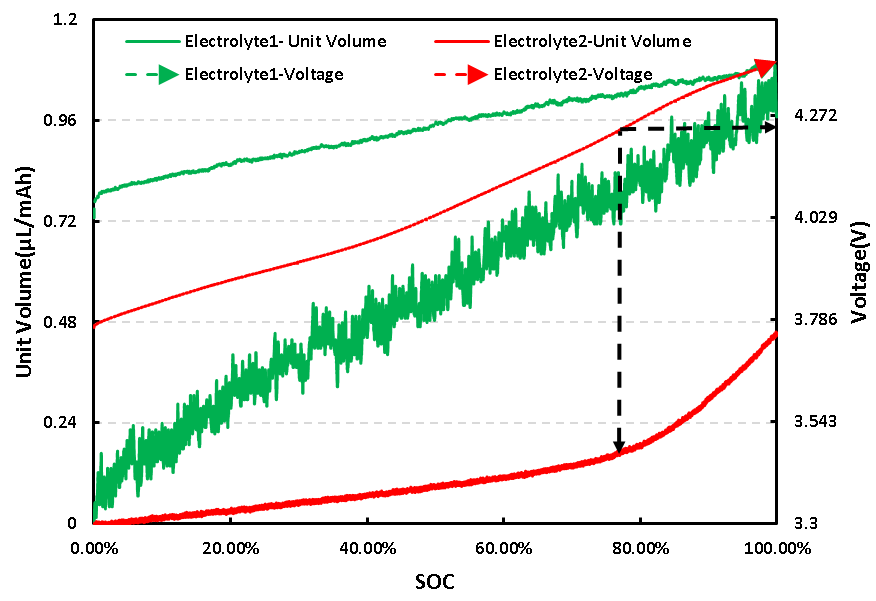
图4. 两种电解液体系电芯充电电压及单位体积变化曲线
2.不同电解液体系电芯产气成分分析
采用气相色谱法分别对两种电解液体系充电后的电芯进行气相成分分析,取出1mL的气体,采用气相色谱进行定性分析,如图5为不同电解液体系的产气成分分析图,对比分析发现,相比Electrolyte1体系,加入添加剂后的Electrolyte2体系产气类别上CO2明显降低,而CO明显增多。
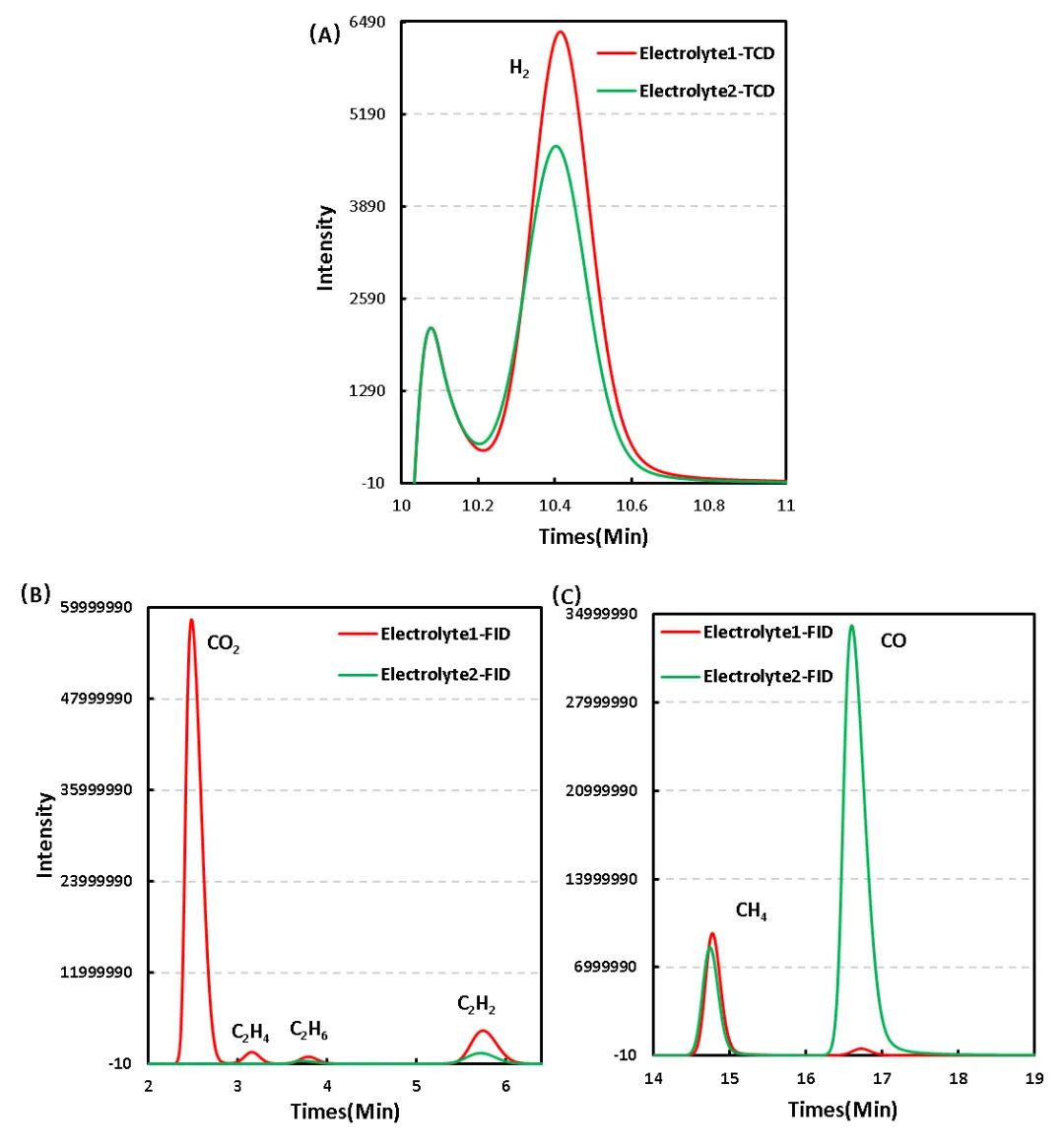
图5. 不同电解液体系产气成分差异:TCD&FID
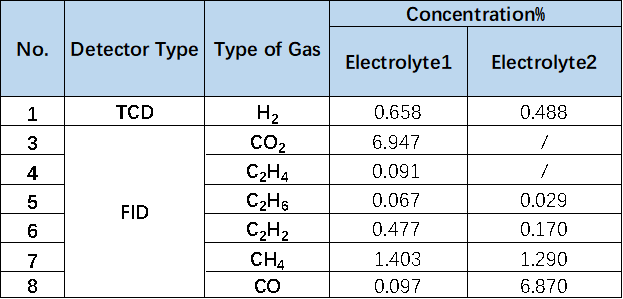
为进一步明确两种电解液体系产气差异,对其产气类型及浓度进行了对比分析,如表1及图6所示, Electrolyte1体系充电后CO2浓度为6.949%,而加入添加剂后的Electrolyte2体系CO2浓度几乎为0。
据相关研究报道CO2是正极反应的主要气体【2】,而正极产气主要是正极材料与电解液的副反应产生的,一方面来自于正极表面Li2CO3的分解,另一方面电池充电到比较高的电压时NCM材料的表面开始释放原子氧,强氧化性的原子氧会导致电解液的氧化分解,产生CO2和CO;产生的H2主要来自于电解液中残留的水分;这说明Electrolyte2电解液中添加剂可能是一种有效的正极成膜添加剂,可以在正极表面形成稳定的保护膜,进而有效减少正极与电解液副反应的发生, 同样的C2H4和C2H2浓度的减少也和该体系下正极的反应变化相关联。
CO等气体主要是负极成膜的过程中,电解液中的EC溶剂在负极表面发生分解导致的;对于与负极反应相关的CO浓度变化,相比Electrolyte1体系CO浓度0.097%,Electrolyte2体系加入添加剂后CO的浓度增长到了6.870%,由于负极材料在电芯体系产气反应中受温度的影响很大,由此看来,Electrolyte2体系中添加剂的加入会降低负极的热稳定性,加速高温下副反应的发生。
除此之外,其它几种类型的气体浓度也会有不同的差异,这种差异除了电解液体系差异外,还可能与电芯组装差异有关。
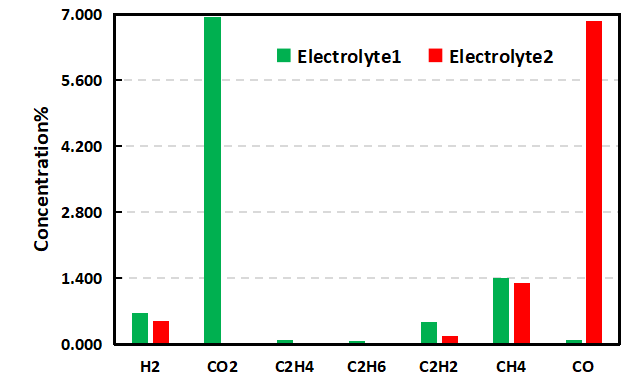
图6. 不同电解液体系产气类型浓度对比图
表1. 不同电解液体系产气类型浓度对比表格
总结
本文采用一种可控温双通道原位产气体积监控仪,并结合气相色谱,对比不同电解液体系下NCM对Li体系电池产气行为及产气成分差异,进一步明确了添加剂对电芯内部电化学反应的差异,同时印证了该分析系统可作为电解液配方优化及添加剂性能评估及优化筛选的有效手段。
审核编辑:刘清
